Livre blanc :
Synthèse organique pilotée par l'intelligence artificielle - En route vers la synthèse autonome ?
Adapté de
C. Empel, R. M. Koenigs, Angew. Chem. Int. Ed. 2019, 58, 17114. https://doi.org/10.1002/anie.201911062
Publié avec l'aimable autorisation de Wiley.
La créativité et la discipline méticuleuse des chimistes organiques ont permis la synthèse organique de molécules complexes pendant des décennies et leur synthèse est souvent appelée "l'art de la synthèse." Des algorithmes d'intelligence artificielle sont développés et affinés non seulement pour effectuer des recherches bibliographiques et des analyses rétrosynthétiques, mais aussi pour identifier et classer les voies de synthèse potentielles incluant les conditions de réaction. Embel et Koenigs passent en revue un article récent de Science qui combine le développement de plans de synthèse pour les petites molécules, piloté par l'intelligence artificielle (IA), avec un processus de synthèse automatisé développé par l'IA. Ils discutent également de ses limites et soulignent les innovations futures qui permettront d'améliorer les avantages de la synthèse organique pilotée par l'IA.
Introduction
Traditionnellement, la synthèse totale de molécules complexes, y compris la synthèse organique, implique de la créativité, une évaluation méticuleuse de chaque étape pour le rendement du produit souhaité, et un processus réitératif pour modifier les réactions pour des propriétés biochimiques ou biologiques spécifiques (par exemple, la biodisponibilité, la solubilité) et optimiser les rendements. L'IA est utilisée pour proposer des méthodes de réaction telles que de nouvelles voies de synthèse de composés. Empel et Koenigs suggèrent que la prochaine étape de l'évolution de l'IA serait la synthèse automatisée en plusieurs étapes de molécules complexes. Bien que similaires, les synthèses automatisées et autonomes se distinguent par la nécessité d'une intervention humaine. Lors de la synthèse automatisée, l'intervention humaine est nécessaire pour définir les seuils, les limites, les paramètres de réaction et les protocoles de synthèse dans les fichiers de réaction. En revanche, la synthèse autonome est un processus synthétique autogéré qui s'adapte aux paramètres environnants, tels que la stéréosélectivité et le rendement de la réaction, sans intervention humaine.
Limites de l'analyse rétrosynthétique traditionnelle et de la synthèse automatisée
Sans le soutien de l'IA, les chimistes peuvent facilement manquer des combinaisons pertinentes de nouveaux substrats, l'optimisation des réactions, la conception de catalyseurs améliorés et de nouvelles réactions dans le corpus de la littérature chimique qui s'étend rapidement. Toutes les disciplines des sciences chimiques considèrent la synthèse de petites molécules comme un goulot d'étranglement et la synthèse automatisée à la demande peut aider à surmonter ce défi.
Les composés peu solubles posent des défis supplémentaires dans les workflows automatisés et nécessitent souvent plus d'intervention humaine pour améliorer le processus en raison de l'obstruction des canaux. Les prévisions sur la solubilité des réactifs dans le plan de synthèse proposé restent limitées, ce qui entrave l'exécution Article 18 Vert de certaines voies synthétiques. Les réactions qui nécessitent ou produisent des températures subambiantes ont généralement aussi besoin des conseils d'un chimiste expert pour maintenir un Workflow efficace. Après la synthèse automatisée, une purification par lots sera nécessaire pour le composé final et peut nécessiter un équipement spécial tel que des colonnes particulières.
AI-Planification des voies de synthèse et synthèse automatisée
Embel et Koenigs résument l'article récent de Jamison et Jensen et de leurs collègues [1]. Ils ont combiné la planification de la rétrosynthèse assistée par ordinateur et un appareil à flux robotiquement reconfigurable pour fournir une synthèse à la demande de petites molécules (50-750 g/mole), comme le résume la figure 1. Le système nécessite encore une intervention humaine pour compléter l'algorithme synthétique de l'IA avec des considérations pratiques (par exemple, stéréochimie précise et choix des solvants) qui aident à optimiser le processus de synthèse en plusieurs étapes.
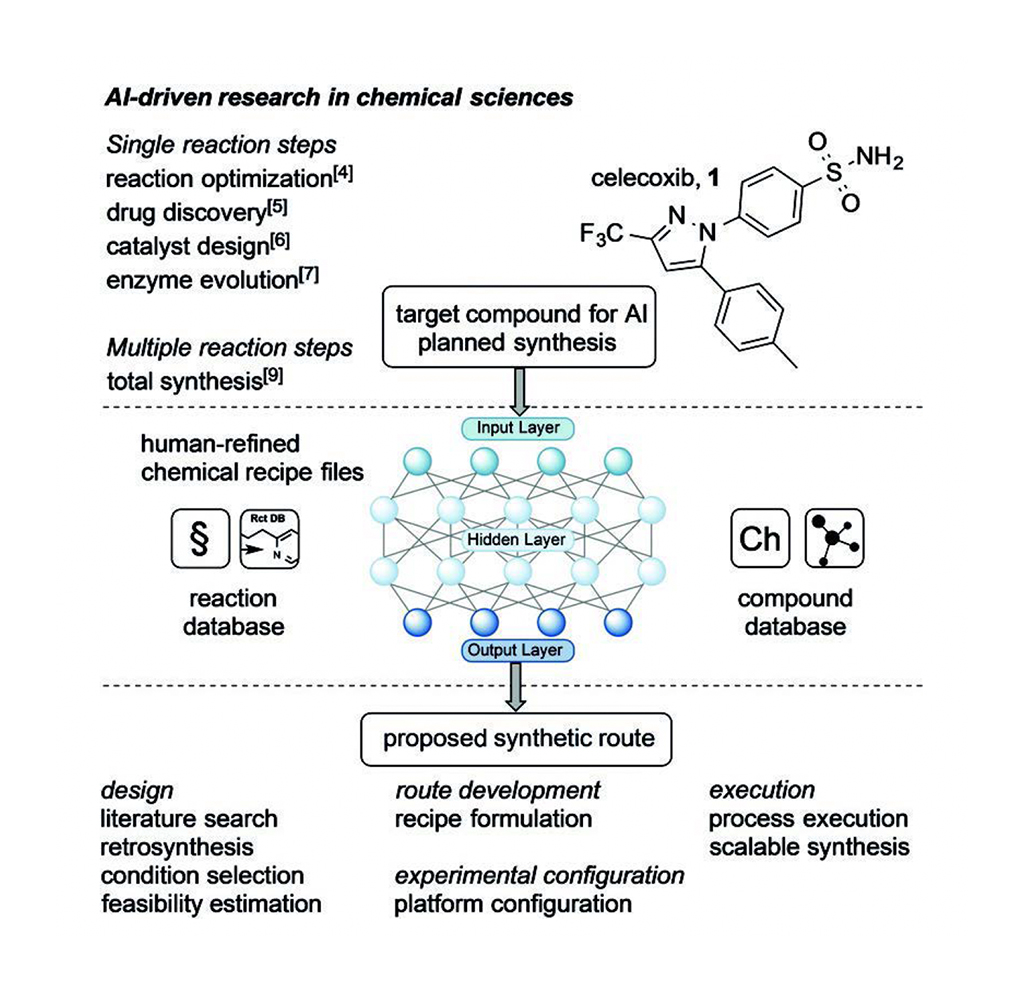
L'IA apprend les principes de conception à partir d'une recherche documentaire dans des bases de données qui incluent des réactions de rétrosynthèse et des réactions de composés apparentés pour concevoir une ou plusieurs voies de synthèse. Les plans proposés incluent les conditions de réaction, les précurseurs, les enzymes (si nécessaire), les catalyseurs, les substrats, les précurseurs et les sous-produits à chacune des étapes. L'IA fournit également une estimation de la faisabilité de chaque plan de synthèse proposé afin que le(s) chimiste(s) puisse(nt) choisir le plan le plus approprié pour l'automatisation, souvent en microfluidique, avec l'intention de mettre le processus à l'échelle. Après que l'IA a développé un plan de synthèse in silico à partir des bases de données de réactions et de composés, les chimistes utilisent leurs connaissances expertes de la synthèse pour affiner les fichiers de recettes chimiques, ainsi que les configurations expérimentales et de plate-forme. Les chimistes ajustent les fichiers de recettes pour pallier les insuffisances des systèmes de flux microfluidiques avant qu'ils ne soient utilisés dans une baie chimique du système automatisé. Ainsi, l'apport des chimistes facilite la mise en œuvre robotique de la synthèse en plusieurs étapes proposée, ce qui constitue une étape majeure vers la synthèse évolutive.
Jamison, Jensen et leurs collègues ont utilisé cette stratégie pour prédire les voies de synthèse de novo de 15 petites molécules, modifier les fichiers de recettes pertinents et automatiser leur synthèse à l'aide de flux de travail microfluidiques [1]. Les 15 composés comprennent l'anti-inflammatoire non stéroïdien (AINS) célécoxib, l'anticoagulant warfarine et le promédicament de l'inhibiteur de l'ECA, le quinapril. La figure 2 (panneau supérieur) illustre le processus de synthèse de l'anti-inflammatoire non stéroïdien (AINS) célécoxib (structure 1). Les deux premières travées de réaction commandées par robot ont réalisé la condensation de Claisen de l'acétophénone 4-méthyle (2) avec le trifluoroacétate de méthyle (3). Une autre baie de réaction commandée par robot a effectué la condensation finale de l'intermédiaire avec l'hydrazine (4) et a produit le célécoxib.
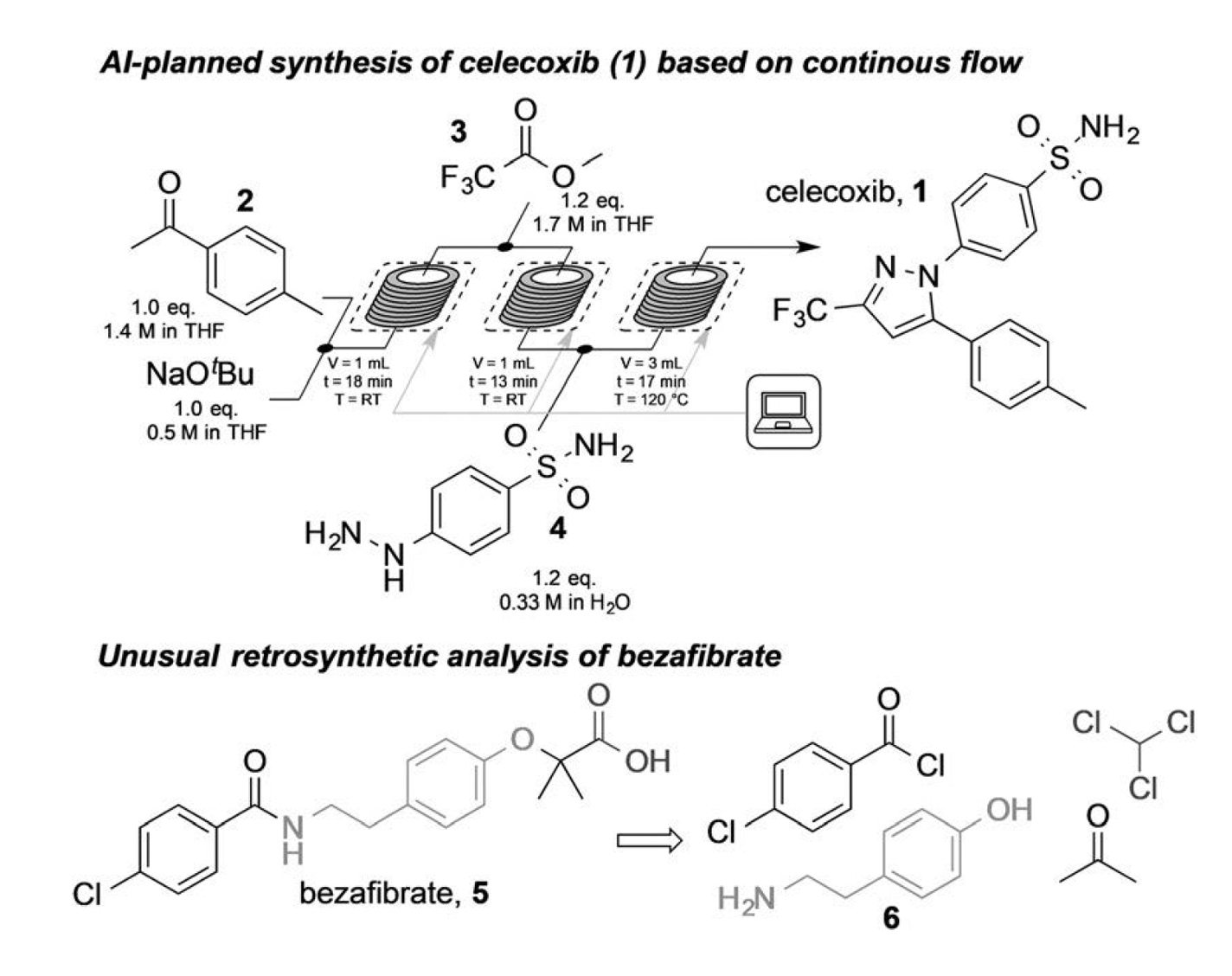
Jamison, Jensen et leurs collègues ont appliqué la technologie pilotée par l'IA pour développer des plans de synthèse et l'exécution synthétique de plusieurs inhibiteurs de l'ECA et de nombreux analogues du célécoxib [1]. Le rendement des petites molécules allait de 342 mg/h à 572 mg/h.
Le plan de synthèse proposé par l'IA pour le bézafibrate utilisait une réaction de Bargellini impliquant l'acétone, le chloroforme et le phénol (6). Cependant, des températures inférieures à la température ambiante ont été observées lors de la tentative de synthèse du bézafibrate (Fig. 2 compound 5) par microfluidique. Jamison, Jensen et leurs collègues ont démontré la faisabilité du plan de synthèse proposé par l'IA en effectuant un processus de synthèse manuel distinct. Le rendement était de 76 %.
Améliorations futures
De multiples groupes travaillent à l'amélioration de l'analyse prédictive de la stéréochimie pilotée par l'IA et des méthodes visant à favoriser la structure stéréochimique souhaitée dans la synthèse proposée. Cette amélioration pourrait réduire l'intervention humaine nécessaire pour la ou les modifications et l'utilisation des fichiers de recettes chimiques.
À l'avenir, l'IA pourrait également être en mesure de proposer des schémas de purification en continu ou des systèmes de purification par lots afin de fournir un composé cible relativement pur. L'ajout d'analyses de réaction en ligne pourrait fournir des informations importantes sur la progression de la réaction et permettre aux algorithmes de rétroaction de modifier les paramètres de réaction en temps réel et d'améliorer potentiellement l'efficacité et le rendement.
Résumé
Jamison, Jensen et leurs collègues ont décrit leur synthèse à la demande de petites molécules (50-750 g/mole) pilotée par l'IA en combinant la planification de la rétrosynthèse assistée par ordinateur avec des fichiers de réaction affinés par des chimistes qui dirigent un appareil à flux robotiquement reconfigurable [1]. Ils ont utilisé cette stratégie pour prédire les voies de synthèse de novo de 15 petites molécules, modifier les fichiers de recettes pertinents et automatiser leur synthèse à l'aide de workflows microfluidiques. Les 15 composés comprennent l'anti-inflammatoire non stéroïdien (AINS) célécoxib, l'anticoagulant warfarine et le promédicament de l'inhibiteur de l'ECA, le quinapril. Embel et Koenigs ont évoqué des limitations telles que la faible solubilité d'un ou de plusieurs composants et les composés cibles nécessitant une stéréochimie spécifique. Ils ont également suggéré d'étendre les plans proposés pilotés par l'IA pour inclure des schémas de purification et/ou des analyses de réaction en cours de processus afin d'automatiser davantage le processus de synthèse. Ces améliorations permettraient de confier le travail de synthèse et d'optimisation de routine à des robots afin que les chimistes puissent consacrer davantage d'efforts à des projets de recherche motivés par la curiosité, à la surveillance et à l'analyse approfondies des réactions et à des découvertes fortuites.
Références
[1] Coley, C.W. et al. (2019). Une roboticplatform pour la synthèse en flux de composés organiques informée par la planification de l'IA. Science.DOI : 10.1126/science.aax1566.
