White Paper:
Künstliche Intelligenz-gesteuerte organische Synthese - Auf dem Weg zur autonomen Synthese?
Angepasst von
C. Empel, R. M. Koenigs, Angew. Chem. Int. Ed. 2019, 58, 17114. https://doi.org/10.1002/anie.201911062
Veröffentlicht mit freundlicher Genehmigung von Wiley.
Die Kreativität und akribische Disziplin der organischen Chemiker ermöglichen seit Jahrzehnten die organische Synthese komplexer Moleküle, und ihre Herstellung wird oft als "die Kunst der Synthese" bezeichnet. Algorithmen der künstlichen Intelligenz werden entwickelt und verfeinert, um nicht nur Literaturrecherchen und retrosynthetische Analysen durchzuführen, sondern auch um potenzielle Syntheserouten zu identifizieren und in eine Rangfolge zu bringen, die die Reaktionsbedingungen einschließt. Embel und Koenigs besprechen einen aktuellen Science-Artikel, der die von Künstlicher Intelligenz (KI) gesteuerte Entwicklung von Syntheseplänen für kleine Moleküle mit einem von KI entwickelten automatisierten Syntheseprozess kombiniert. Sie erörtern auch die Grenzen dieses Verfahrens und weisen auf künftige Innovationen hin, mit denen die Vorteile der KI-gesteuerten organischen Synthese verbessert werden können.
Einleitung
Traditionell erfordert die Gesamtsynthese komplexer Moleküle, einschließlich der organischen Synthese, Kreativität, eine sorgfältige Bewertung jedes einzelnen Schritts im Hinblick auf die Ausbeute des gewünschten Produkts und einen wiederholten Prozess zur Modifizierung der Reaktionen für bestimmte biochemische oder biologische Eigenschaften (z. B. Bioverfügbarkeit, Löslichkeit) und zur Optimierung der Ausbeute. Die KI wird eingesetzt, um Reaktionsmethoden vorzuschlagen, z. B. neue Wege für die Synthese von Verbindungen. Empel und Koenigs schlagen vor, dass der nächste Evolutionsschritt in der KI die automatisierte mehrstufige Synthese komplexer Moleküle sein könnte. Obwohl sie sich ähneln, unterscheiden sich automatisierte und autonome Synthese durch den Bedarf an menschlichem Input. Bei der automatisierten Synthese sind menschliche Eingaben erforderlich, um Schwellenwerte, Grenzen, Reaktionsparameter und Syntheseprotokolle in den Reaktionsdateien zu definieren. Im Vergleich dazu ist die autonome Synthese ein sich selbst steuernder Syntheseprozess, der sich ohne menschliche Eingaben an die Umgebungsparameter wie Stereoselektivität und Reaktionsausbeute anpasst.
Grenzen der traditionellen retrosynthetischen Analyse und der automatisierten Synthese
Ohne KI-Unterstützung können Chemiker in der schnell wachsenden chemischen Literatur leicht relevante Kombinationen neuartiger Substrate, Reaktionsoptimierung, das Design verbesserter Katalysatoren und neuartige Reaktionen übersehen. Die Synthese kleiner Moleküle stellt in allen Disziplinen der chemischen Wissenschaften einen Engpass dar, und die automatisierte On-Demand-Synthese kann helfen, diese Herausforderung zu bewältigen.
Schlecht lösliche Verbindungen stellen in automatisierten Arbeitsabläufen eine zusätzliche Herausforderung dar und erfordern oft mehr menschliche Eingriffe zur Verbesserung des Prozesses, da sie die Kanäle verstopfen. Vorhersagen über die Löslichkeit der Reaktanten im vorgeschlagenen Syntheseplan sind nach wie vor begrenzt, was die Ausführung einiger Syntheserouten erschwert . Reaktionen, die subambiente Temperaturen erfordern oder ergeben, bedürfen in der Regel ebenfalls der Beratung durch einen erfahrenen Chemiker, um einen effizienten Workflow zu gewährleisten. Nach der automatisierten Synthese muss die endgültige Verbindung im Batch-Verfahren gereinigt werden, wofür unter Umständen spezielle Geräte wie besondere Säulen erforderlich sind.
AI-Planung von Synthesewegen und automatisierte Synthese
Embel und Koenigs fassen den jüngsten Artikel von Jamison und Jensen und ihren Kollegen [1] zusammen. Sie kombinierten eine computergestützte Retrosynthese-Planung mit einer robotergestützten rekonfigurierbaren Fließapparatur, um eine On-Demand-Synthese kleiner Moleküle (50-750 g/Mol) zu ermöglichen (siehe Abbildung 1). Das System erfordert nach wie vor menschliche Eingaben, um den KI-Synthesealgorithmus mit praktischen Überlegungen zu ergänzen (z. B. präzise Stereochemie und Wahl des Lösungsmittels), die zur Optimierung des mehrstufigen Syntheseprozesses beitragen.
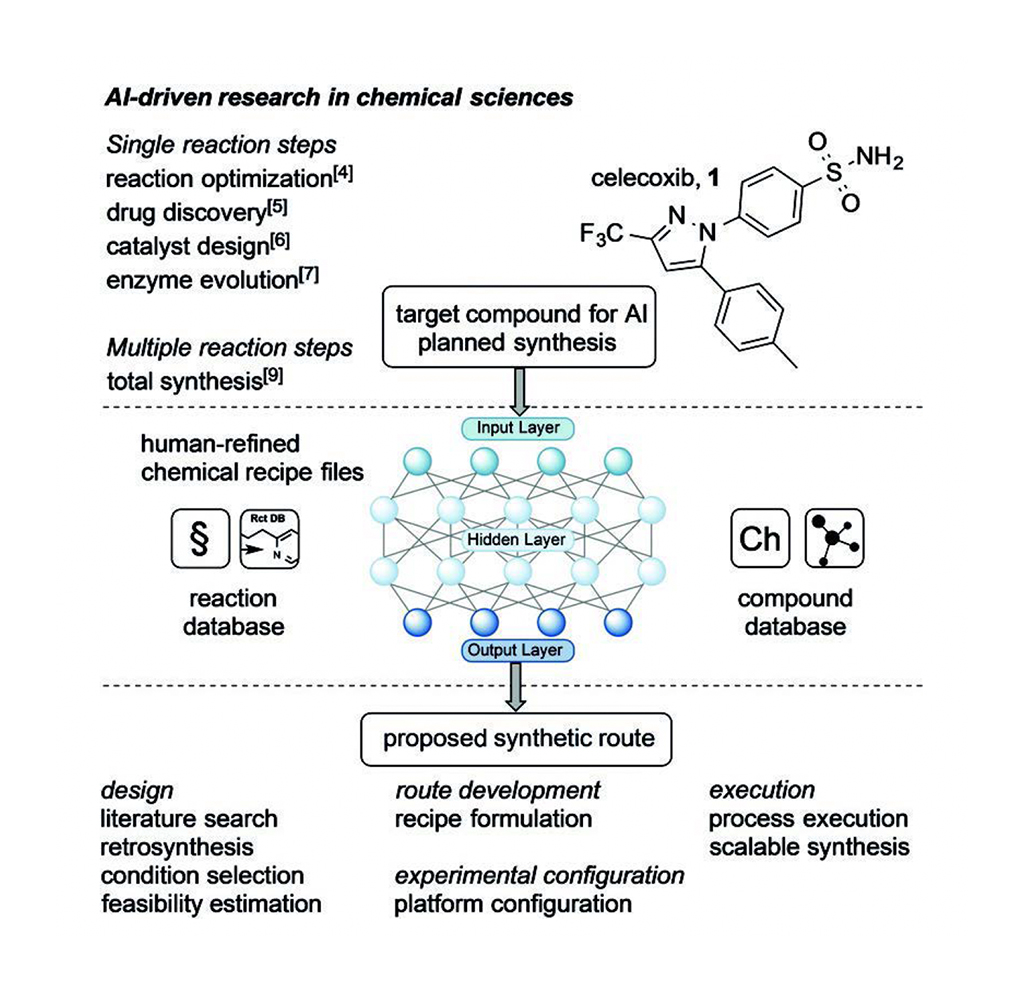
KI erlernt Konstruktionsprinzipien aus einer Literatursuche in Datenbanken, die Retrosynthesereaktionen und verwandte Verbindungsreaktionen enthalten, um eine oder mehrere synthetische Routen zu entwerfen. Die vorgeschlagenen Pläne enthalten Reaktionsbedingungen, Vorläufer, Enzyme (je nach Bedarf), Katalysatoren, Substrate, Vorläufer und Nebenprodukte in jedem der Schritte. AI liefert auch eine Einschätzung der Durchführbarkeit jedes vorgeschlagenen Syntheseplans, so dass der/die Chemiker den am besten geeigneten Plan für die Automatisierung, häufig in der Mikrofluidik, auswählen können, um den Prozess zu skalieren. Nachdem KI aus den Reaktions- und Verbindungsdatenbanken einen In-silico-Syntheseplan entwickelt hat, verfeinern die Chemiker mit ihrem Fachwissen über Synthese die chemischen Rezeptdateien sowie die Versuchs- und Plattformkonfigurationen. Die Chemiker passen die Rezeptdateien an, um etwaige Unzulänglichkeiten der mikrofluidischen Durchflusssysteme zu beheben, bevor sie in einer chemischen Bucht im automatisierten System verwendet werden. Auf diese Weise erleichtern die Eingaben der Chemiker die robotergestützte Umsetzung der vorgeschlagenen mehrstufigen Synthese, was einen wichtigen Schritt in Richtung skalierbarer Synthese darstellt.
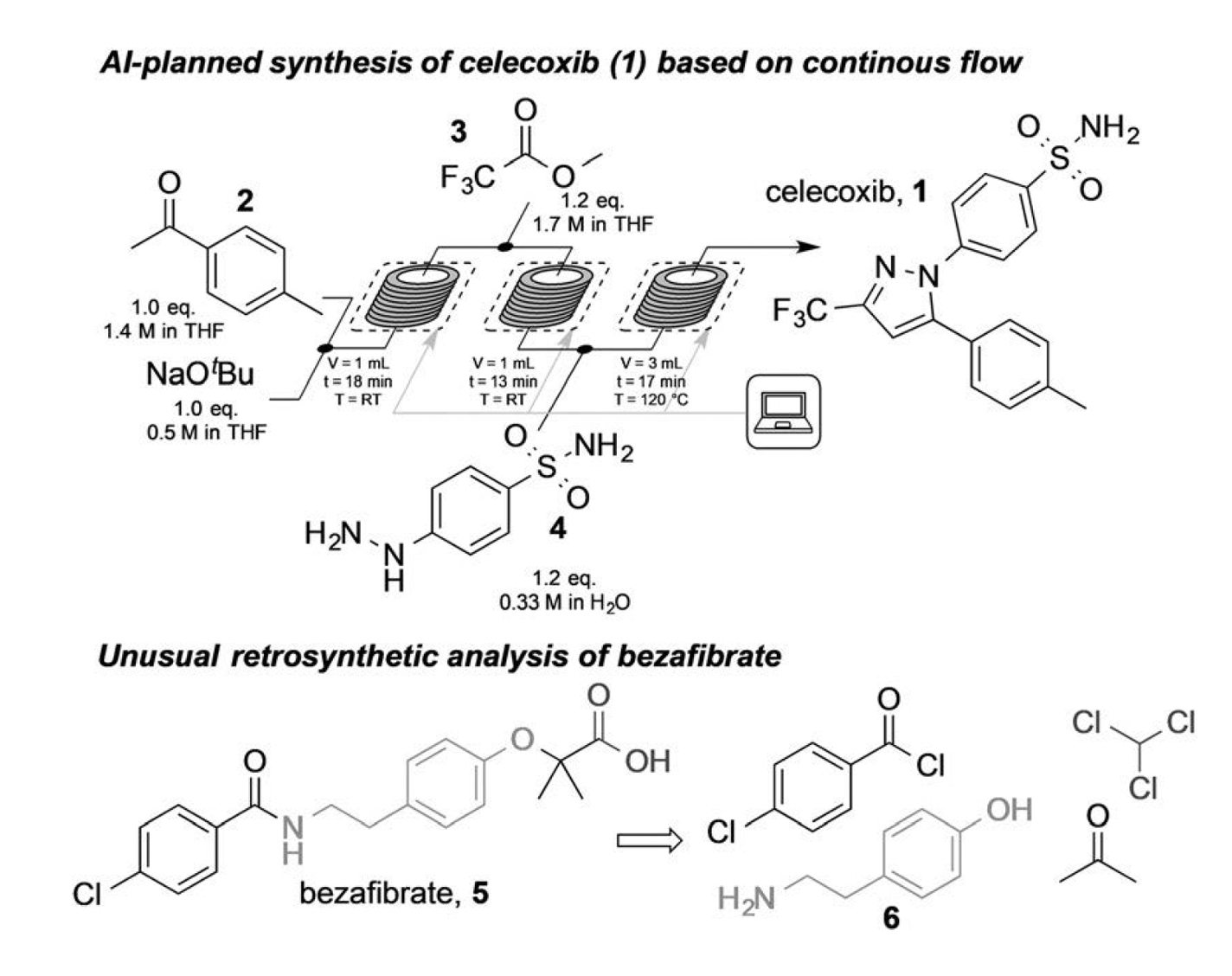
Jamison, Jensen und Kollegen nutzten diese Strategie, um de novo-Syntheserouten für 15 kleine Moleküle vorherzusagen, die entsprechenden Rezeptdateien zu modifizieren und ihre Synthese mithilfe mikrofluidischer Workflows zu automatisieren [1]. Zu den 15 Verbindungen gehören der nichtsteroidale Entzündungshemmer (NSAID) Celecoxib, der Blutverdünner Warfarin und der ACE-Hemmer Prodrug, Quinapril. Abbildung 2 (oben) zeigt den Syntheseprozess für das nichtsteroidale Antirheumatikum (NSAID) Celecoxib (Struktur 1). In den ersten beiden robotergesteuerten Reaktionsfeldern wurde die Claisen-Kondensation von 4-Methylacetophenon (2) mit Methyltrifluoracetat (3) durchgeführt. Ein weiteres robotergesteuertes Reaktionsfeld führte die endgültige Kondensation des Zwischenprodukts mit Hydrazin (4) durch und lieferte Celecoxib.
Jamison, Jensen und Kollegen wandten die KI-gesteuerte Technologie an, um Synthesepläne zu entwickeln und die Synthese mehrerer ACE-Hemmer und zahlreicher Celecoxib-Analoga durchzuführen [1]. Die Ausbeute der kleinen Moleküle reichte von 342 mg/h bis 572 mg/h.
Der von AI vorgeschlagene Syntheseplan für Bezafibrat verwendete eine Bargellini-Reaktion mit Aceton, Chloroform und Phenol (6). Bei der versuchten Synthese von Bezafibrat (Abb. 2 Verbindung 5) mittels Mikrofluidik traten jedoch Temperaturen unterhalb der Umgebungstemperatur auf. Jamison, Jensen und Kollegen demonstrierten die Durchführbarkeit des von AI vorgeschlagenen Syntheseplans, indem sie einen separaten manuellen Syntheseprozess durchführten. Die Ausbeute betrug 76 %.
Zukünftige Verbesserungen
Mehrere Gruppen arbeiten an der Verbesserung der KI-gesteuerten Analyse und Vorhersage der Stereochemie und der Methoden, um die gewünschte stereochemische Struktur in der vorgeschlagenen Synthese zu begünstigen. Diese Verbesserung könnte die für die Modifizierung(en) und die Verwendung der chemischen Rezeptdateien erforderlichen menschlichen Eingaben reduzieren.
In Zukunft könnte die KI auch in der Lage sein, kontinuierliche Reinigungsschemata oder Batch-Reinigungssysteme vorzuschlagen, um eine relativ reine Zielverbindung zu erhalten. Eine zusätzliche Online-Reaktionsanalyse könnte wichtige Informationen über den Reaktionsfortschritt liefern und es den Feedback-Algorithmen ermöglichen, die Reaktionsparameter in Echtzeit zu ändern und die Effizienz und Ausbeute potenziell zu verbessern.
Zusammenfassung
Jamison, Jensen und Kollegen beschrieben ihre KI-gesteuerte On-Demand-Synthese kleiner Moleküle (50-750 g/mol) durch die Kombination computergestützter Retrosyntheseplanung mit chemisch verfeinerten Reaktionsdateien, die eine robotergestützte rekonfigurierbare Fließapparatur steuern [1]. Sie nutzten diese Strategie, um de novo-Syntheserouten für 15 kleine Moleküle vorherzusagen, die entsprechenden Rezeptdateien zu modifizieren und ihre Synthese mithilfe mikrofluidischer Workflows zu automatisieren. Zu den 15 Verbindungen gehören der nichtsteroidale Entzündungshemmer (NSAID) Celecoxib, der Blutverdünner Warfarin und der ACE-Hemmer Prodrug, Quinapril. Embel und Koenigs erörterten Einschränkungen wie die schlechte Löslichkeit einer oder mehrerer Komponenten und Zielverbindungen, die eine spezifische Stereochemie erfordern. Sie schlugen außerdem vor, die KI-gesteuerten vorgeschlagenen Pläne um Reinigungsschemata und/oder prozessinterne Reaktionsanalysen zu erweitern, um den Syntheseprozess weiter zu automatisieren. Diese Verbesserungen würden die routinemäßige Synthese- und Optimierungsarbeit auf Roboter verlagern, so dass Chemiker mehr Zeit für neugierige Forschungsprojekte, gründliche Reaktionsüberwachung und -analyse sowie für zufällige Entdeckungen aufwenden können.
Referenzen
[1] Coley, C.W. et al. (2019). A roboticplatform for flow synthesis of organic compounds informed by AI planning. Science.DOI: 10.1126/science.aax1566.
