Libro blanco:
Automatizaciones sintéticas: Una revolución de la Edad de Piedra a la Era Moderna
Adaptado de
Fang, G., Lin, D.-Z. y Liao, K. (2023), Synthetic Automations: A Revolution From "Stone Age" to Modern Era. Chin. J. Chem., 41: 1075-1079. https://doi.org/10.1002/cjoc.202200713
Publicado con la cortesía de Wiley.
La síntesis orgánica tradicional ha hecho progresos sobresalientes, pero la operación manual, la reproducibilidad inconsistente y la eficiencia inadecuada obstaculizan su evolución fiable hacia la automatización inteligente. La química sintética está empezando a adoptar programas informáticos de Inteligencia artificial (IA) para sustituir procesos laboriosos como la investigación para el desarrollo de posibles vías sintéticas, la identificación de reactivos de reacción con opciones clasificadas de planes putativos de síntesis orgánica y la síntesis automatizada. En este artículo, Liao y sus colegas destacan algunos de los avances más representativos de la síntesis automatizada y presentan los retos actuales y las orientaciones futuras en este campo.
Antecedentes
La revolución industrial de los siglos XVIII y XIX fue testigo del poder de la fabricación automatizada. La síntesis orgánica ha dependido de mano de obra altamente cualificada (químicos) para crear y realizar el proceso de ensamblaje molecular. En la década de 1960, Merrifield informó del primer sistema automatizado en química orgánica: la síntesis de péptidos en fase sólida mediante la fijación del C-terminal a una resina y el enmascaramiento del N-terminal con un grupo protector. El sistema de automatización bombea los reactivos y disolventes pertinentes, los mezcla con la resina y los retira en el orden correcto para lograr la desprotección, la acilación, la separación y las purificaciones.
En la mayoría de los casos, la síntesis orgánica sigue siendo un proceso que requiere mucho tiempo y trabajo y que ofrece resultados variables debido a las diferencias en las técnicas de distintos laboratorios e instalaciones. En este Tema Emergente, Fang y sus colegas destacan varios avances recientes, como la investigación impulsada por la IA, la planificación de la síntesis asistida por IA y la automatización robótica integrada en IA del proceso de síntesis propiamente dicho. También se exponen los retos que plantean el diseño y la aplicación de las vías sintéticas automatizadas.
Breakthroughs
Muchos fármacos son moléculas pequeñas con estructuras químicas diversas y, por tanto, requieren procedimientos personalizados que consumen tanto dinero como mano de obra altamente cualificada. Burke desarrolló una estrategia iterativa de ensamblaje de catalizadores de carbono 2D y cobalto 3D (C-Csp2, C-Csp3) y automatizó el proceso para sintetizar 14 clases diversas de moléculas pequeñas. El uso de ácido tetrametil N-metiliminodiacético (TIDA) favoreció la formación de enlaces C-Csp3. Esta máquina de síntesis, combinada con más de 5.000 bloques de construcción comerciales, podría facilitar la síntesis de numerosas moléculas pequeñas.
Las plataformas de síntesis basadas en flujo pueden proporcionar un control preciso de las temperaturas de reacción, los tiempos de reacción y la composición, y pueden desempeñar un papel importante en la síntesis automatizada. Por ejemplo, el dispositivo de flujo rápido Tiny Tides inventado por Li y Pentelute et al. podría producir de forma eficiente ácido nucleico peptídico conjugado con péptidos de penetración celular [1]. Mo et al. aceleraron el descubrimiento de nuevos procesos electroorgánicos con experimentos de alto rendimiento en su plataforma microfluídica automatizada de cribado y análisis de una sola gota en 2020 [2]. En 2022, Wang et al. diseñaron una plataforma de pruebas de electrocatalizadores: Realizó 942 pruebas efectivas de 109 catalizadores bimetálicos basados en cobre en 55 horas [3].
Gilmore y colaboradores desarrollaron un sintetizador automatizado de múltiples pasos que podía proporcionar de forma estable y reproducible procesos sintéticos tanto lineales como convergentes mediante la disposición de múltiples módulos de flujo continuo alrededor de un núcleo central [4]. El cambio de un módulo a otro no requería configuración manual. El instrumento también incluía monitorización en línea con resonancia magnética nuclear (RMN) y espectroscopia infrarroja (IR): la monitorización facilitaba el análisis posterior a la reacción y la retroalimentación. Demostraron la flexibilidad de la configuración de flujo radial sintetizando una biblioteca de derivados del anticonvulsivo rufinamida.
El grupo de Mo describió una plataforma automatizada que recogía estimaciones de polaridad mediante cromatografía en capa fina (TLC) en línea en 2022 [5]. La plataforma de IA entrenada podía estimar la probabilidad de separación de múltiples compuestos y ayudar a proponer condiciones de purificación.
Para minimizar la necesidad de aportaciones de químicos humanos, el grupo de Cronin (2019) desarrolló el Chemputer que proporciona instrucciones metodológicas en los pasos individuales e integra la automatización de la plataforma con técnicas a escala de banco utilizando un algoritmo de procesamiento del lenguaje natural (NLP) [6]. El sistema Chemputer podría extraer procedimientos sintéticos de publicaciones, transformar el plan de síntesis en lenguaje de descripción química utilizado para los procedimientos, convertir las instrucciones en comandos para la manipulación de la plataforma automatizada y dirigir la síntesis química. Sin intervención humana, el Chemputer ensambló tres productos farmacéuticos de alta calidad con rendimientos y purezas superiores a los logrados durante los procedimientos manuales de síntesis y purificación Un hito en la automatización de la síntesis química orgánica fue logrado por Coley et al. [7]. Su programa de síntesis química asistida por ordenador incluía una planificación sintética basada en millones de reacciones químicas publicadas y simulaciones in silico para maximizar el éxito. El programa de síntesis IA dirigía una plataforma modular de flujo continuo que ejecutaba la síntesis reconfigurando automáticamente el brazo robótico. Su potencia se demostró planificando y sintetizando 15 compuestos, entre ellos varios inhibidores de la enzima convertidora de angiotensina (ECA) y fármacos AINE.
Grzybowski y Burke et al. describieron un sistema iterativo de aprendizaje automático para explorar las condiciones generales de reacción en el protocolo de síntesis automatizada propuesto [8]. Un sencillo flujo de trabajo en bucle cerrado aprovechó la matriz guiada por datos aprendida por máquina para priorizar y seleccionar las reacciones subsiguientes para las pruebas, y utilizó la experimentación robótica para aumentar la precisión, el rendimiento y la reproducibilidad. Su flujo de trabajo mediante experimentación y aprendizaje automático identificó las condiciones de reacción para la reacción de acoplamiento hetero(aril Suzuki-Miyaura, lo que confirmó su utilidad para las dificultades de optimización química multidimensional.
El grupo de Cooper describió el primer robot móvil integrado en IA que ejecutó de forma autónoma 688 reacciones a lo largo de ocho días para probar a fondo diez variables de forma experimental [9]. Sin embargo, el robot no tenía capacidad de software para captar el conocimiento químico existente, ni aprendizaje automático para generar hipótesis científicas novedosas.
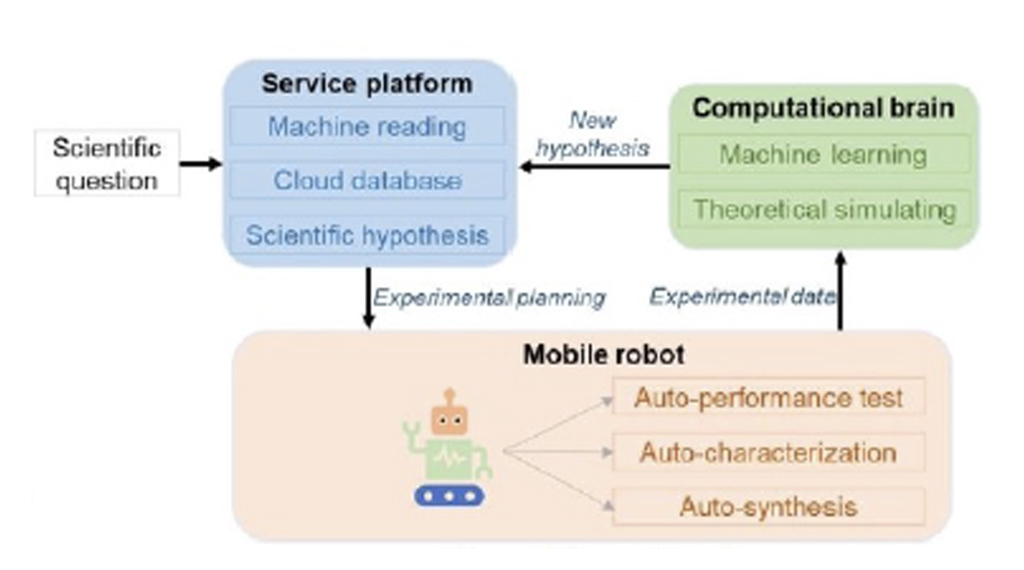
El grupo de Jiang (2022) describió una plataforma de IA, denominada AI-Chemist, que podía realizar los pasos esenciales para proponer y clasificar la planificación sintética, la ejecución de los pasos sintéticos, la monitorización y la recopilación de datos del proceso de síntesis a través de múltiples reacciones y pasos, y el aprendizaje automático (Fig. 1) [10].
Retos y perspectivas
Se ha avanzado mucho en las plataformas automáticas y autónomas impulsadas por IA para la síntesis orgánica. Sin embargo, su adopción generalizada se aceleraría si se abordaran los siguientes retos.
Integración perfecta de la plataforma sintética automatizada, que contiene módulos para el almacenamiento de reactivos, módulo de preparación de reacciones, numerosos módulos de reactores, instrumento(s) analítico(s) integrado(s) para la monitorización de las reacciones, sistema de purificación, sistema de gestión de compuestos, unidad de monitorización y consola. Debido a las limitaciones de espacio en la mayoría de los laboratorios, lo ideal sería que el tamaño de los instrumentos y de la plataforma no superase el de una campana extractora. El algoritmo o algoritmos de planificación de la síntesis asistida por ordenador o por IA deben integrarse a la perfección con la plataforma de síntesis química asistida por ordenador (CASP) y el equipo de monitorización.
La plataforma física y el software deben ser fácilmente personalizables y reconfigurables para usos futuros.
La unidad completa debe tener un precio razonable (bajo), ya que muchos laboratorios contratarían a químicos reales en lugar de unidades de automatización con costes similares.
La plataforma de automatización y el software deben ser fáciles de usar: sencillos en la configuración y optimización de la planificación/clasificación sintética y en la selección y ejecución del proceso sintético. El uso de un lenguaje de programación química universal para la entrada y recuperación de datos por parte de los químicos ayudará a maximizar su beneficio para los químicos humanos.
A medida que se extienda el uso de la automatización de la síntesis química orgánica, los químicos orgánicos se verán liberados de la experimentación repetitiva utilizada a menudo durante la optimización. Los químicos orgánicos podrán dedicar más tiempo a responder a las preguntas "¿Qué debemos sintetizar? ¿Por qué?", en lugar de dedicarse a la mecánica de la síntesis en sí.
Resumen
Múltiples grupos están avanzando en la síntesis de química orgánica impulsada por la IA, acoplando el aprendizaje automático para proponer y probar experimentalmente nuevas rutas sintéticas prometedoras de forma automática sin necesidad de intervención humana. La síntesis automatizada puede mejorar los rendimientos de forma fiable y liberar a los químicos de tareas manuales rutinarias para que puedan centrarse en tareas creativas.
Referencias
[1] Li, C. et al. (2022). Automated Flow Synthesis of Peptide-PNA Conjugates. ACS Central Science. DOI: 10.1021/acscentsci.1c01019.
[2] Mo, Y. et al. (2020). A Multifunctional Microfluidic Platform for Alto rendimiento Experimentation of Electroorganic Chemistry. Angewandte Chemie - International Edition. DOI: 10.1002/ anie.202009819.
[3] Xie, M. et al. (2022). Fast Screening for Copper-Based Bimetallic Electrocatalysts: Efficient Electrocatalytic Reduction of CO2 to C2+ Products on Magnesium-Modified Copper. Angewandte Chemie - International Edition. DOI: 10.1002/anie.202213423.
[4] Chatterjee, S. et al. (2020). Síntesis radial automatizada de moléculas orgánicas. Nature. DOI: 10.1038/s41586-020- 2083-5.
[5] Xu, H. et al. (2022). High-throughput discovery of chemical structure-polarity relationships combining automation and machine-learning techniques. Chem. DOI: 10.1016/j.chempr.2022.08.008.
[6] Steiner, S. et al. (2019). Síntesis orgánica en un sistema robótico modular dirigido por un lenguaje de programación química. Science. DOI: 10.1126/science.aav2211.
[7] Coley, C.W. et al. (2019). Una plataforma robótica para la síntesis de flujo de compuestos orgánicos informada por la planificación de IA. Science. DOI: 10.1126/science.aax1566.
[8] Angello, N.H. et al. (2022). Closed-loop optimization of general reaction conditions for heteroaryl Suzuki-Miyaura coupling. Science. DOI: 10.1126/science. adc8743.
[9] Burger, B. et al. (2020). A mobile robotic chemist. Nature. DOI: 10.1038/s41586- 020-2442-2.
10] Zhu, Q. et al. (2022). Una IA-química polifacética con mente científica. Revista Nacional de Ciencia. DOI: 10.1093/ nsr/nwac190.
